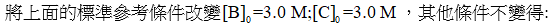"以Excel程式模擬反應速率" 修訂間的差異
| 行 1: | 行 1: | ||
<div style="float:left;"> | <div style="float:left;"> | ||
| − | <font color="black" size="4"> | + | <font color="black" size="4">震盪反應是一類非常特別的化學反應,原因是反應過程中某一或多種分子的濃度會隨時間反覆地增減。藉由Excel程式模擬震盪反應,我們可以讓同學經由改變實驗條件,了解震盪反應的內涵。                  <br></font><br> |
<br><br> | <br><br> | ||
| 行 8: | 行 8: | ||
<hr> | <hr> | ||
| − | ==1. | + | ==1.說明 == |
| − | + | 震盪反應的過程中,某一或多種分子的濃度會隨時間反覆地增減。震盪反應曾引起化學家們極大的興趣,某一分子的濃度在反應中反覆循環,與傳統的化學反應非常不同。 | |
<br><br> | <br><br> | ||
| − | == | + | ==2.教學目標 == |
| − | + | 在實驗室中我們操作過震盪反應(若時間充裕可加做BZ反應)之後,可以利用Excel程式模擬震盪反應過程,模擬可以讓同學改變實驗條件,包括反應物起始濃度,以及速率常數。 | |
| − | |||
| − | |||
| − | |||
| − | |||
<br><br> | <br><br> | ||
| − | ==3. | + | ==3.實驗步驟 == |
| − | *3. | + | *3.1 設計「回饋」反應,並將模擬結果與沒有回饋機制的反應比較: |
| + | ::<img style="width:600px;" src='https://upload.wikimedia.org/wikipedia/commons/0/0e/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E9%9C%87%E7%9B%AA%E5%8F%8D%E6%87%891.png'/> | ||
| − | + | ::<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/0/0e/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E9%9C%87%E7%9B%AA%E5%8F%8D%E6%87%892.png'/> | |
| − | |||
| − | |||
| − | |||
| − | + | ::<img style="width:400px;" src='https://upload.wikimedia.org/wikipedia/commons/1/18/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E9%9C%87%E7%9B%AA%E5%8F%8D%E6%87%893.png'/> | |
| − | :: | + | ::<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/5/59/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E9%9C%87%E7%9B%AA%E5%8F%8D%E6%87%894.png'/> |
| − | :: | + | ::可以看出,回饋機制使得[A]緩慢增加,無回饋機制時[A]則隨時間遞減,且後者達平衡所需時間約為前者的一半。 |
| − | + | ||
| − | : | + | *3.2 設計多步驟「循環回饋」反應: |
| − | |||
| − | ::<img style="height: | + | ::最容易製造出震盪反應的是以下的想像實驗 |
| − | < | + | ::<img style="height:200px;" src='https://upload.wikimedia.org/wikipedia/commons/9/9d/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E9%9C%87%E7%9B%AA%E5%8F%8D%E6%87%895.png'/> |
| − | :: | + | ::其中,反應物和產物相互抵消,因此是一個「零」反應,而每一格個別反應都包含了回饋機制。 |
| + | ::以標準參考條件: | ||
| + | ::<img style="width:600px;" src='https://upload.wikimedia.org/wikipedia/commons/b/b1/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E9%9C%87%E7%9B%AA%E5%8F%8D%E6%87%896.png'/>,所得的濃度與時間相關圖如下: | ||
| + | ::<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/c/c3/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E9%9C%87%E7%9B%AA%E5%8F%8D%E6%87%897.png'/> | ||
| + | ::三種分子的濃度隨時間以不同的週期震盪,且濃度變化顯示反應漸趨平衡。 | ||
| − | ::<img style=" | + | *3.3 三種分子的起始濃度與速率常數對震盪周期的影響: |
| − | + | ::<img style="width:400px;" src='https://upload.wikimedia.org/wikipedia/commons/c/c3/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E9%9C%87%E7%9B%AA%E5%8F%8D%E6%87%898.png'/> | |
| − | |||
| − | ::<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/ | + | ::<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/6/62/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E9%9C%87%E7%9B%AA%E5%8F%8D%E6%87%899.png'/> |
| − | |||
| − | + | ::<img style="width:500px;" src='https://upload.wikimedia.org/wikipedia/commons/f/f4/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E9%9C%87%E7%9B%AA%E5%8F%8D%E6%87%8910.png'/> | |
| − | |||
| − | |||
| − | |||
| − | + | ::<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/a/a1/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E9%9C%87%E7%9B%AA%E5%8F%8D%E6%87%8911.png'/> | |
| − | :: | + | ::三種反應物起始濃度相同(3.0 M)時,震盪週期改變,達到平衡的時間變短。 |
<br><br> | <br><br> | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | ==4.分析與評量 == | |
| − | + | *4.1 在這個模擬中,如果假設性地改變某一反應條件(如反應物的濃度或速率常數),你能先猜出可能的震盪趨勢嗎? | |
| − | + | *4.2 如果改變一組兩組或三組反應的反應及逆反應速率常數的數值及相對值,紀錄震盪趨勢如何隨之改變。 | |
| + | *4.3 從以上的探索,試歸納出何種條件可以設計出震盪趨勢最明顯(及最不明顯)的反應條件。 | ||
<br><br> | <br><br> | ||
| − | |||
| − | |||
| − | + | ==5.參考文獻 == | |
| − | |||
| − | :: | + | *[1] 震盪反應: http://highscope.ch.ntu.edu.tw/wordpress/?p=18914http://inside.mines.edu/~dwu/classes/CH353/labs/ClockCKS/Wet%20Lab%204/Oscillating%20Reactions.pdf |
| − | + | *[2] BZ反應: https://zh.wikipedia.org/wiki/B-Z%E5%8F%8D%E5%BA%94 | |
| − | + | *[3] Oregonator震盪反應模擬: http://www.scholarpedia.org/article/Oregonator | |
| − | |||
| − | |||
| − | |||
| − | |||
<br><br> | <br><br> | ||
| − | ==6. | + | ==6.進階探索 == |
| − | *6.1 | + | *6.1 綜合以上分析,試推論何種條件可以讓震盪週期增長。 |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
<br><br><br><br><br><br><br> | <br><br><br><br><br><br><br> | ||
於 2019年8月6日 (二) 16:31 的修訂
震盪反應是一類非常特別的化學反應,原因是反應過程中某一或多種分子的濃度會隨時間反覆地增減。藉由Excel程式模擬震盪反應,我們可以讓同學經由改變實驗條件,了解震盪反應的內涵。
1.說明
震盪反應的過程中,某一或多種分子的濃度會隨時間反覆地增減。震盪反應曾引起化學家們極大的興趣,某一分子的濃度在反應中反覆循環,與傳統的化學反應非常不同。
2.教學目標
在實驗室中我們操作過震盪反應(若時間充裕可加做BZ反應)之後,可以利用Excel程式模擬震盪反應過程,模擬可以讓同學改變實驗條件,包括反應物起始濃度,以及速率常數。
3.實驗步驟
- 3.1 設計「回饋」反應,並將模擬結果與沒有回饋機制的反應比較:
- 可以看出,回饋機制使得[A]緩慢增加,無回饋機制時[A]則隨時間遞減,且後者達平衡所需時間約為前者的一半。
- 3.2 設計多步驟「循環回饋」反應:
- 最容易製造出震盪反應的是以下的想像實驗

- 其中,反應物和產物相互抵消,因此是一個「零」反應,而每一格個別反應都包含了回饋機制。
- 以標準參考條件:
 ,所得的濃度與時間相關圖如下:
,所得的濃度與時間相關圖如下:
- 三種分子的濃度隨時間以不同的週期震盪,且濃度變化顯示反應漸趨平衡。
- 3.3 三種分子的起始濃度與速率常數對震盪周期的影響:
- 三種反應物起始濃度相同(3.0 M)時,震盪週期改變,達到平衡的時間變短。
4.分析與評量
- 4.1 在這個模擬中,如果假設性地改變某一反應條件(如反應物的濃度或速率常數),你能先猜出可能的震盪趨勢嗎?
- 4.2 如果改變一組兩組或三組反應的反應及逆反應速率常數的數值及相對值,紀錄震盪趨勢如何隨之改變。
- 4.3 從以上的探索,試歸納出何種條件可以設計出震盪趨勢最明顯(及最不明顯)的反應條件。
5.參考文獻
- [1] 震盪反應: http://highscope.ch.ntu.edu.tw/wordpress/?p=18914http://inside.mines.edu/~dwu/classes/CH353/labs/ClockCKS/Wet%20Lab%204/Oscillating%20Reactions.pdf
- [2] BZ反應: https://zh.wikipedia.org/wiki/B-Z%E5%8F%8D%E5%BA%94
- [3] Oregonator震盪反應模擬: http://www.scholarpedia.org/article/Oregonator
6.進階探索
- 6.1 綜合以上分析,試推論何種條件可以讓震盪週期增長。