動手學科學/物質科學I/物質的組成
目錄
開場
- 看一下課程簡介
- 練習使用「網路檔案櫃」
- 區網 wifi :jendo_c,密碼現場說明
本日活動
一、穿不過去
(一)先備知識
- 原子半徑/原子核半徑比例,「鈾」的是26634倍,而「氫」是60250倍,平均是43442倍。原子核(10-15M)如果放大到一個人的大小,原子核之間的距離大約是台北到新竹間的距離。
- 拉塞福用阿爾法粒子打白金箔紙,每8000個阿爾法粒子,就有一個粒子會大角度散射,而其它粒子都直直地衝過白金箔紙。
(二)操作
- 請兩組同學各推派一位代表,各自決定自己的方向和位置,且彼此不能溝通。但維持和老師溝通。
- 請老師指導,不斷調整兩位同學的位置和方向,直到兩位同學的向前方向會彼此相交為止。
- 請上述兩組同學擔任示範組,每位同學均扮演「固體的原子核」:
- 每一組同學扮演一件「固體」的原子核。
- 由上一點的代表同學為中心,同組同學用皮尺維持間距 10 公尺,並對齊排列,模擬固體表面。
- 請同學想像:事實上,下一顆原子核應該遠在新竹而不是 10 公尺外。
- 兩組同學(兩件固體)相向運動,每運動一步,就與同組同學對齊一次。
- 觀察兩組同學是否會進入彼此固體表面的內部。
- 活動照片
| 學員依模擬距離分開站 | 往對面移動 | 交錯而過 |
|---|---|---|
|
|
|
|
(三)探究問題
觀察並探討為何原子核間距很寬,兩件固體相向運動時卻不會穿過對方。
- Ans:
- 中間的區域同時存在著電子。
- 因為包立不相容原理,已滿的電子軌域無法容納更多電子,因此兩個原子會因為彼此的電子軌域互相排斥而不會穿透。
請簡單解釋包立不相容原理。
- Ans:
- 任意兩個處於同一原子軌道的兩個電子不能佔有相同的量子態。
- 處於同一原子軌道的兩個電子自旋方向必定相反。
如果人如原子核的大小,電子的大小還小於一元的銅板,在台北與新竹間放20個一元銅板,即使它們能繞行原子核運動,它們能擋住固體表面相互進入彼此內部嗎?
- Ans: 可以,因為包立部相容原理。
二、粒子、波雙重性
(一)先備知識
- 光子和電子都具有:粒子/波雙重性,會出現類似的雙狹縫干涉條紋。
- 都遵守:λ =h/p ,波長=普朗克常數/動量
- 對光子來說波振輻的大小代表電磁場的大小。
- 對電子來說,波振輻的平方等於等於電子出現的機率。
| 紅光 | 綠光 | 藍光 | 用200伏特加速的電子 | 用200伏特加速的質子 | 秒速40米150克的棒球 |
|---|---|---|---|---|---|
| 7×10-7 | 5.3×10-7 | 4.6×10-7 | 8.7×10-11 | 2×10-12 | 1.1×10-34 |
- 在微觀世界中,電子是可以「同時」出現在甲地,也「同時」出現在乙地,只是分別在甲地與乙地被找到的機率各有不同,其出現機率由波函數表達。
- 1927年,貝爾實驗室將電子射向鎳結晶,發現其繞射圖譜電子被證實有波的性質。
- 速度以每秒40米,質量為0.15公斤的棒球,其波長為 10-34 ,比原子核還要小很多很多,根本測不出來。
- 1999年,富勒烯被測出有波的性質。

(二)操作
- 每組發一隻雷射筆,一張紙,一支 0.5 mm 自動鉛筆芯,夾子大小各一,同學自備可調焦距的手機。
- 每組三人以上分工,一人持夾子和雷射筆,並持筆芯中分雷射筆;一人拿紙和尺,映照出雙狹縫干涉條紋,並用刻度尺對準干涉圖樣;一人用手機拍下來。
- 算出干涉條紋間隔。
- 運用公式:
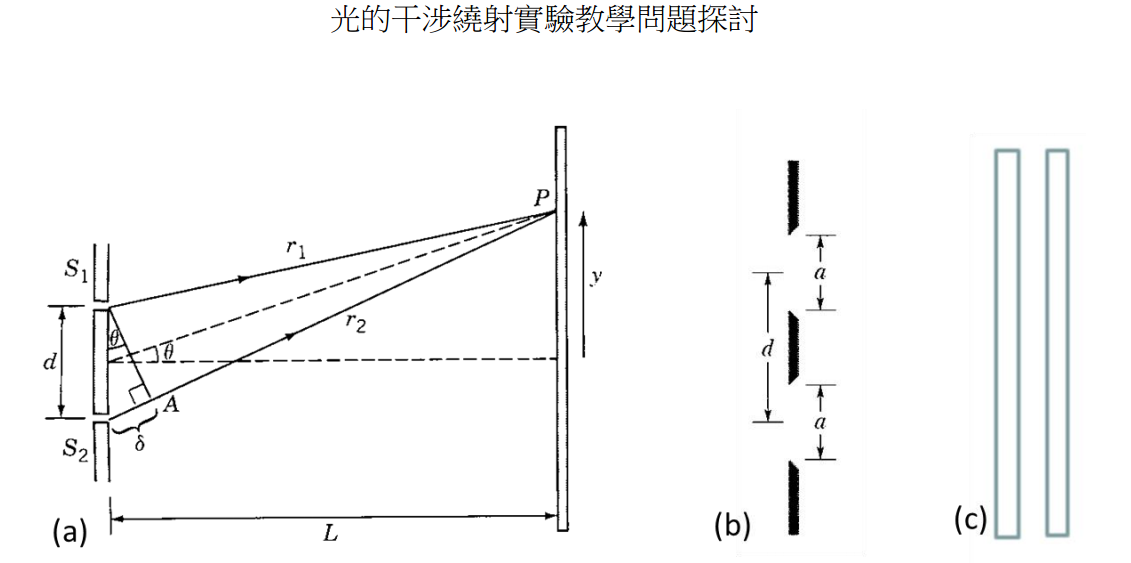
- 光程差(1波長)/狹縫間距(0.5mm)=sinθ ≈ tanθ=亮紋間隔/筆紙間距(約四米)
- 活動照片
| 實驗材料 | 筆芯史雷射光產生雙狹縫干涉 | 量測干涉條紋間距 |
|---|---|---|
|
|
|
|
- 注意:筆芯貼著雷射筆筆尖,垂直對準雷射筆中央,盡量剛好把雷射光切一半
(三)探究問題
請拍照上傳過程與結果照片。
- Ans: 略
在紙上端正寫出組內分工以及計算波長的算式,並上傳照片。
- Ans: 略
討論各組結果為何不同?
- Ans: 實驗中有各種不同的誤差。
踢除極端值,全班各組做平均。
- Ans: 略
上網查出綠光雷射的波長,並跟實驗數據做比較。
- Ans: 比較誤差大小,是否在兩個數量級以內。
三、電子軌域勞作
一、先備知識
- 包立不相容原理:兩個全同的費米子(如電子)不能處於相同的量子態。=>兩個量子組態一樣的電子,不能存在於相同的軌域中。
- 原子的電子軌域:第一層為 1S ,球形;第二層為 2S,2Px,2Py,2Pz;第三層為 3S,3Px,3Py,3Pz,其他軌域先忽略。
- s:1種形狀,球狀對稱

- p:3種p軌域,形狀一樣但方向不同

- 同層 S,Px,Py,Pz

- s:1種形狀,球狀對稱
- 更完整的電子軌域圖示:
.jpg)
元素電子組態 s1 s2 1 氫
1.0082 氦
4.003s1 s2 p1 p2 p3 p4 p5 p6 3 鋰
6.9414 鈹
9.0125 硼
10.816 碳
12.017 氮
14.018 氧
16.009 氟
19.0010 氖
20.1811 鈉
22.9912 鎂
24.3113 鋁
26.9814 矽
28.0915 磷
30.9716 硫
32.0717 氯
35.4518 氬
39.9519 鉀
39.120 鈣
40.08二、操作
- 每組發電子軌域紙、剪刀、雙面膠共用
- 參考前人的模型
- 組合出二氧化碳…等分子:H2,O2,H2O,CO2,CH4
- 組合出金屬導線,並用以解釋電流為什麼可以輕易在金屬中流動。
- 對照球桿模型,做出H2,O2,H2O,CO2,CH4等分子
H2(氫) O2(氧) H20(水) CO2(二氧化碳) CH4(甲烷) 




常見分子
去 http://jendo.org/wiki1231/index.php?title=化學鍵#.E5.90.84.E7.A8.AE.E5.88.86.E5.AD.90 參看更多種常見分子,可以試著組組看哦!
三、探究問題
將立體的S,Px,Py,Pz 的原子外圍電子軌域,簡化成紙本平面的四個軌域,會有哪些模擬不完整的地方?
- Ans: 平面與立體的差別
固體表面為什麼不會互相浸入的問題?
- Ans: 包立不相容原理。
金屬為什麼有導電的特性?
- Ans:
- 導電的特性為電子容易移動。
- 金屬元素最外層的軌域,都有很多空間可以讓電子進入,因此當很多個金屬原子連在一起時,就會形成一個通道方便電子移動。





