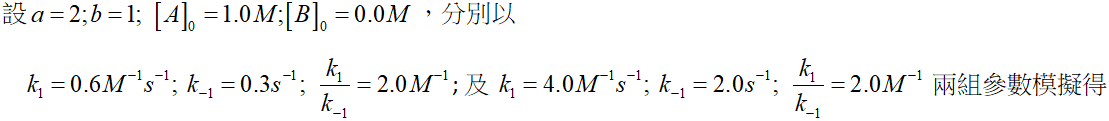"以Excel程式模擬化學平衡" 修訂間的差異
(已建立頁面,內容為 "<div style="float:left;"> <font color="black" size="4">藉由Excel程式模擬反應物及產物與時間的關係,經由改變各種實驗條件,了解化學平…") |
|||
| 行 32: | 行 32: | ||
:<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/5/54/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A16.png'/> | :<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/5/54/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A16.png'/> | ||
:可以看出,反應時間約 6 sec 時正、逆反應速率相等。反應商定義為 | :可以看出,反應時間約 6 sec 時正、逆反應速率相等。反應商定義為 | ||
| − | ::::::<img style="width: | + | ::::::::<img style="width:100px;" src='https://upload.wikimedia.org/wikipedia/commons/1/1e/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A17.png'/> |
:反應商與時間之關係如下: | :反應商與時間之關係如下: | ||
:<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/3/37/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A18.png'/> | :<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/3/37/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A18.png'/> | ||
| − | :<img style=" | + | :<img style="width:500px;" src='https://upload.wikimedia.org/wikipedia/commons/0/09/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A19.png'/> |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| + | *3.2 影響反應達平衡所需時間之因素(正、逆反應皆為一次反應) : | ||
| + | :::::<img style="height:70px;" src='https://upload.wikimedia.org/wikipedia/commons/5/59/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A121.png'/> | ||
| + | :*3.2.1 改變反應物起始濃度 :<img style="width:100px;" src='https://upload.wikimedia.org/wikipedia/commons/e/eb/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A110.png'/> : [A] 、[B] 與時間之關係圖,正、逆反應速率與時間之關係圖,反應商與時間之關係圖分別為 | ||
| + | ::<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/2/29/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A111.png'/>:<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/1/15/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A112.png'/> | ||
| + | ::<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/f/f6/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A113.png'/> | ||
| + | :在[A] 、[B] 與時間之關係圖及正、逆反應速率與時間之關係圖中,所有的數據都是原反應條件的兩倍,反應商與時間之關係圖則和原反應條件數據相同。 | ||
| + | *3.3 影響反應達平衡所需時間之因素(正反應為二次反應、逆反應為一次反應) : | ||
| + | :::::<img style="height:70px;" src='https://upload.wikimedia.org/wikipedia/commons/5/55/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A114.png'/> | ||
| + | :*3.3.1 反應物起始濃度分別為<img style="width:200px;" src='https://upload.wikimedia.org/wikipedia/commons/0/04/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A115.png'/> 及 ,反應商與時間之關係圖分別為 | ||
| + | ::<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/6/66/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A116.png'/> | ||
| + | ::起始濃度低時,達平衡所需時間較長。 | ||
| + | :*3.3.2 | ||
| + | ::::<img style="width:800px;" src='https://upload.wikimedia.org/wikipedia/commons/1/14/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A117.png'/> | ||
| + | ::<img style="height:300px;" src='https://upload.wikimedia.org/wikipedia/commons/e/e4/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A118.png'/> | ||
| + | ::對於平衡常數相同的反應,正、逆反應速率較大時達平衡所需時間較短。 | ||
| + | *3.4 影響反應達平衡所需時間之其他因素: | ||
| + | :學生試寫出其他可設定的參數 ,整理出影響平衡時間的因素 。 | ||
<br><br> | <br><br> | ||
==4.分析與結論 == | ==4.分析與結論 == | ||
| − | *4. | + | *4.1 影響平衡所需時間的因素(起始濃度): |
| − | + | :<img style="width:400px;" src='https://upload.wikimedia.org/wikipedia/commons/e/eb/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A119.png'/> | |
| − | + | *4.2 影響平衡所需時間的因素(速率常數): | |
| − | + | :<img style="width:400px;" src='https://upload.wikimedia.org/wikipedia/commons/7/78/%E4%BB%A5Excel%E7%A8%8B%E5%BC%8F%E6%A8%A1%E6%93%AC%E5%8C%96%E5%AD%B8%E5%B9%B3%E8%A1%A120.png'/> | |
| − | + | ||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
<br><br> | <br><br> | ||
| 行 65: | 行 69: | ||
*5.1 能實際撰寫Excel程式、從數據、繪製圖表 。 | *5.1 能實際撰寫Excel程式、從數據、繪製圖表 。 | ||
*5.2 能從圖表或的結論,並能合理化解釋 。 | *5.2 能從圖表或的結論,並能合理化解釋 。 | ||
| − | *5. | + | *5.3能了解「化學平衡」之意涵,化學反應平衡時正、逆反應仍然持續進行,正、逆反應速率相等。 |
| − | *5. | + | *5.4化學平衡時正、逆反應速率相等,反應商達固定值,即平衡常數。 |
| + | |||
<br><br> | <br><br> | ||
==6.參考資料 == | ==6.參考資料 == | ||
*6.1參考文獻 | *6.1參考文獻 | ||
| − | + | :[1] 化學平衡: https://en.wikipedia.org/wiki/Chemical_equilibrium | |
| − | + | :[2] 平衡常數: https://en.wikipedia.org/wiki/Equilibrium_constant | |
| − | : | + | |
| − | |||
於 2019年9月24日 (二) 06:23 的最新修訂
藉由Excel程式模擬反應物及產物與時間的關係,經由改變各種實驗條件,了解化學平衡(chemical equilibrium)的內涵。化學反應達平衡時正反應速率等於逆反應速率,且平衡常數等於逆反應速率常數除以正反應速率常數。
1.現象說明
在學習化學平衡的過程中,學習者接觸的核心概念包括正、逆反應速率常數、反應級數等。Excel程式是學習反應速率的最佳工具,因為我們可以引入「一段極短時間」的概念,改變反應條件進行探索,計算濃度與時間、反應速率與時間、反應商 (reaction quotient, Qr) 與時間的關係。
2.探究問題
利用Excel程式,改變實驗條件,包括反應物濃度、反應級數、反應速率常數,讓學習者深入了解化學平衡的內涵。教師可視時間多寡,使用電腦教室讓同學一次或分次自行完成Excel程式,或讓同學使用已完成的程式。過程中探究:
- 2.1 反應速率應如何定義? 反應物與產物的濃度如何表示?
- 2.2 如何在Excel中計算反應速率?
- 2.3 反應商如何隨時間改變,是漸增或漸減呢?
- 2.4 反應商不再改變時,其值等於平衡常數嗎?
- 2.5 平衡常數有沒有單位?
3.實作項目
- 3.1 設定「時間差」(t)及「時間軸」,設一基元反應(elementary reaction) 為
- 基元反應的分子係數即為反應級數,因此正、逆反應速率分別為
- 反應物與產物之濃度與時間的關係分別為


- 正、逆反應速率(rate[for] 、rate[back])與時間之關係如下:
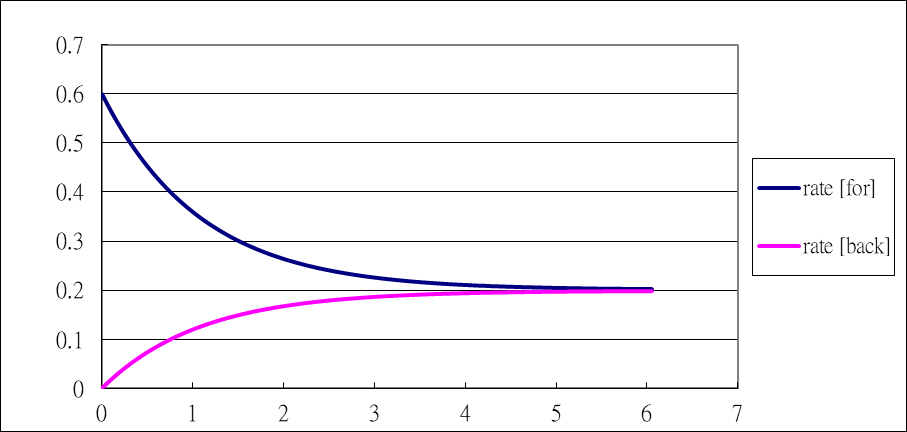
- 可以看出,反應時間約 6 sec 時正、逆反應速率相等。反應商定義為
- 反應商與時間之關係如下:


- 3.2 影響反應達平衡所需時間之因素(正、逆反應皆為一次反應) :
- 3.2.1 改變反應物起始濃度 :
 : [A] 、[B] 與時間之關係圖,正、逆反應速率與時間之關係圖,反應商與時間之關係圖分別為
: [A] 、[B] 與時間之關係圖,正、逆反應速率與時間之關係圖,反應商與時間之關係圖分別為
 :
:

- 在[A] 、[B] 與時間之關係圖及正、逆反應速率與時間之關係圖中,所有的數據都是原反應條件的兩倍,反應商與時間之關係圖則和原反應條件數據相同。
- 3.3 影響反應達平衡所需時間之因素(正反應為二次反應、逆反應為一次反應) :
- 3.3.1 反應物起始濃度分別為
 及 ,反應商與時間之關係圖分別為
及 ,反應商與時間之關係圖分別為

- 起始濃度低時,達平衡所需時間較長。
- 3.3.2

- 對於平衡常數相同的反應,正、逆反應速率較大時達平衡所需時間較短。
- 3.4 影響反應達平衡所需時間之其他因素:
- 學生試寫出其他可設定的參數 ,整理出影響平衡時間的因素 。
4.分析與結論
- 4.1 影響平衡所需時間的因素(起始濃度):
- 4.2 影響平衡所需時間的因素(速率常數):
5.教學目標與評量
- 5.1 能實際撰寫Excel程式、從數據、繪製圖表 。
- 5.2 能從圖表或的結論,並能合理化解釋 。
- 5.3能了解「化學平衡」之意涵,化學反應平衡時正、逆反應仍然持續進行,正、逆反應速率相等。
- 5.4化學平衡時正、逆反應速率相等,反應商達固定值,即平衡常數。
6.參考資料
- 6.1參考文獻
- [1] 化學平衡: https://en.wikipedia.org/wiki/Chemical_equilibrium
- [2] 平衡常數: https://en.wikipedia.org/wiki/Equilibrium_constant